Περιεχόμενο
Κατά τον προσδιορισμό του τυπικού φορτίου ενός μορίου όπως το CoCl2 (αέριο φωσγενίου), πρέπει να γνωρίζετε τον αριθμό των ηλεκτρονίων σθένους για κάθε άτομο και τη δομή Lewis του μορίου.
Ηλεκτρονικός αριθμός Valence
Αναζητήστε κάθε άτομο στον περιοδικό πίνακα των στοιχείων για να καθορίσετε τον αριθμό των ηλεκτρονίων σθένους.
Να θυμάστε ότι δύο ηλεκτρόνια πηγαίνουν στο πρώτο κέλυφος s, δύο ηλεκτρόνια στο δεύτερο κέλυφος s, έξι ηλεκτρόνια στο πρώτο κέλυφος κ, κλπ. Ως υπενθύμιση: 1s (^ 2) 2s (^ 2) 2p (^ 6) ^ 2) 3ρ (^ 6)
Ρυθμίστε τη φόρτιση. Εάν το μόριο είναι ένα ιόν, προσθέστε ή αφαιρέστε ένα ή περισσότερα ηλεκτρόνια συνολικά για να υπολογίσετε την τελική φόρτιση.
Για το CoCl2 (αέριο φωσγενίου): C = 4; Ο = 6; Cl = 7. Το μόριο δεν είναι ιονισμένο και έχει ουδέτερο φορτίο. Επομένως, η συνολική ποσότητα ηλεκτρονίων σθένους είναι 4 + 6 + (7x2) = 24.
Δομή Lewis
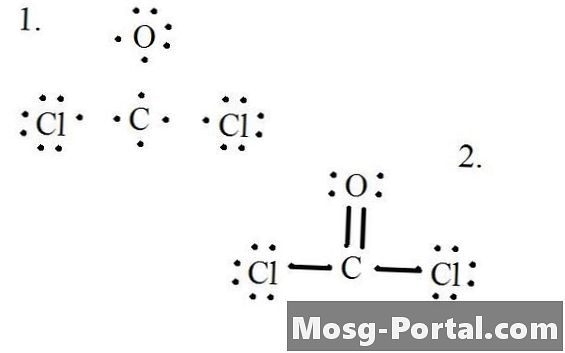
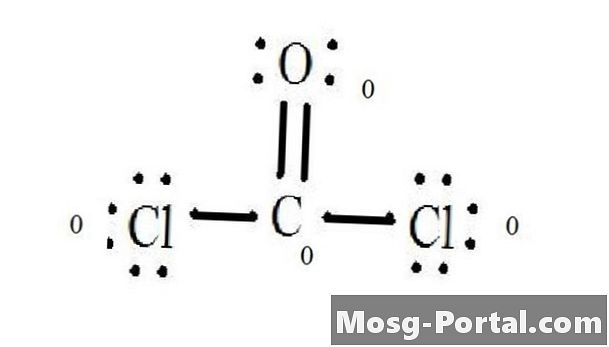
Δείτε το διάγραμμα για τη δομή Lewis του CoCl2 (αέριο φωσγενίου). Η δομή Lewis αντιπροσωπεύει την πιο σταθερή και πιθανή δομή για ένα μόριο. Τα άτομα σχηματίζονται με ζευγαρωμένα ηλεκτρόνια σθένους. οι δεσμοί σχηματίζονται μεταξύ μοναχικών ηλεκτρονίων για να ικανοποιήσουν τον κανόνα των οκτάδων.