Περιεχόμενο
Κάθε στοιχείο έχει έναν μοναδικό αριθμό πρωτονίων στον πυρήνα του, αλλά ο αριθμός των ηλεκτρονίων που βρίσκονται σε τροχιά γύρω του μπορεί να ποικίλει σε κάποιο βαθμό. Τα άτομα διαφέρουν ως προς τον τρόπο που αλληλεπιδρούν με άλλα άτομα και μόρια. Μερικοί τείνουν να προσελκύουν ηλεκτρόνια, ενώ άλλοι τείνουν να εγκαταλείψουν τα ηλεκτρόνια τους. Τέτοιες τάσεις καθορίζουν ποια είδη δεσμών θα σχηματιστούν μεταξύ αλληλεπιδρώντων ατόμων.
Ατομική δομή
Ένα άτομο αποτελείται από σωματίδια γνωστά ως νετρόνια, πρωτόνια και ηλεκτρόνια. Τα πρωτόνια και τα νετρόνια αποτελούν τον πυρήνα των ατόμων, ενώ τα ηλεκτρόνια περιστρέφονται γύρω από αυτό. Τα πρωτόνια είναι θετικά φορτισμένα και τα νετρόνια δεν φορτίζονται. Τα ηλεκτρόνια έχουν αρνητικό φορτίο και αντισταθμίζουν την θετική φόρτιση του πυρήνα. Ένα άτομο που περιέχει ίσο αριθμό πρωτονίων και ηλεκτρονίων δεν έχει καθαρό φορτίο, ένα άτομο που περιέχει περισσότερα ηλεκτρόνια έχει καθαρό αρνητικό φορτίο και ένα άτομο που περιέχει περισσότερα πρωτόνια έχει καθαρό θετικό φορτίο.
Ηλεκτρονίων
Τα ηλεκτρόνια ενός ατόμου δεν περιστρέφονται γύρω από αυτό κατά τρόπο τυχαίο. Αντ 'αυτού, διανέμονται γύρω από τον πυρήνα με πολύ συγκεκριμένους τρόπους. Τα ηλεκτρόνια αποδίδονται σε επίπεδα ενέργειας, με κάθε επίπεδο να σχηματίζει ένα είδος κελύφους γύρω από τον πυρήνα. Μόνο τόσα πολλά ηλεκτρόνια μπορούν να χωρέσουν μέσα σε κάθε κέλυφος και τυχόν επιπλέον ηλεκτρόνια σχηματίζουν το επόμενο κέλυφος. Τα ηλεκτρόνια στο εξωτερικό επίπεδο ενέργειας είναι πολύ σημαντικά.Συμμετέχουν στη συγκόλληση και ονομάζονται ηλεκτρόνια σθένους.
Για περισσότερες πληροφορίες σχετικά με τα ηλεκτρόνια και τα επίπεδα ενέργειας, δείτε το παρακάτω βίντεο:
Ηλεκτροαρνησία
Τα άτομα ορισμένων στοιχείων έχουν μεγαλύτερη τάση να προσελκύουν ηλεκτρόνια και αυτή η ιδιότητα είναι γνωστή ως ηλεκτροαρνητικότητα. Πόσο ένα άτομο προσελκύει ηλεκτρόνια είναι κατά κύριο λόγο μια συνάρτηση του πόσα πρωτόνια βρίσκονται στον πυρήνα και πόσες άλλες ηλεκτρόνια είναι ήδη σε τροχιά. Τα άτομα με περισσότερα πρωτόνια διαθέτουν μεγαλύτερη ποσότητα θετικού φορτίου για να προσελκύσουν επιπλέον ηλεκτρόνια, αλλά μεγαλύτερα άτομα έχουν επίσης ηλεκτρόνια γύρω τους σε διάφορα επίπεδα ενέργειας και αυτά τα ηλεκτρόνια μπορούν να προστατεύσουν οποιαδήποτε πρόσθετα ηλεκτρόνια από τις ελκυστικές δυνάμεις του πυρήνα.
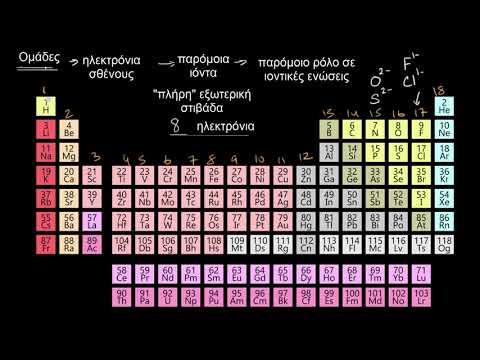
Περιοδικός Πίνακας
Ο περιοδικός πίνακας είναι χρήσιμος για να συμβάλλει στην απεικόνιση των στοιχείων που τείνουν να λαμβάνουν ηλεκτρόνια από άλλα στοιχεία. Όταν κοιτάξετε το τραπέζι και μετακινηθείτε από τα αριστερά προς τα δεξιά σε κάθε σειρά, αυξάνεται ο αριθμός των πρωτονίων σε κάθε στοιχείο. Αυτό σημαίνει ότι το στοιχείο μπορεί να προσελκύσει ηλεκτρόνια πιο έντονα ή είναι πιο ηλεκτροαρνητικό. Αλλά καθώς κατεβαίνετε κάθε στήλη, το στοιχείο αποκτά περισσότερα ενεργειακά επίπεδα και αυτό τείνει να μειώσει τη θετική, ελκυστική έλξη του πυρήνα. Επομένως, τα στοιχεία που συνήθως λαμβάνουν ηλεκτρόνια βρίσκονται γενικά στο δεξιό, ανώτερο τμήμα του περιοδικού πίνακα και περιλαμβάνουν φθόριο, οξυγόνο και άζωτο.